Клинические рекомендации по лечению болей в спине

Высокая распространенность в популяции боли в спине определяет медицинскую и социальную значимость данной проблемы. Боль в спине снижает активность, трудоспособность, ухудшает психоэмоциональное состояние, в отдельных случаях является угрозой для жизни. Согласно статистическим данным, у 15–20% пациентов с острой болью в спине велика вероятность ее хронизации. Это объясняется разными причинами: несвоевременным обращением за медицинской помощью, низким уровнем комплаентности, в отдельных случаях – ошибочными или неадекватными действиями врача. Сложный механизм развития боли в спине, бездоказательное установление причинно-следственной связи между полученными результатами дополнительных методов обследования и клиническими данными, использование традиционных схем лечения независимо от типа боли, недооценка коморбидной патологии затрудняют диагностику и лечение. Все это определяет актуальность проблемы боли в спине в целом и оптимизации диагностических и терапевтических подходов в частности [1–3].
Диагностика
На первом визите на основании детального сбора жалоб, анамнеза, неврологического и, при необходимости, соматического осмотра необходимо определить у пациентов тип боли по этиологии: специфическая, скелетно-мышечная неспецифическая и корешковая.
Причинами специфической боли могут быть заболевание внутренних органов или сосудов (аневризма брюшной аорты), ревматический, воспалительный или инфекционный процесс, первичная или метастатическая опухоль, метаболические нарушения и др. На высокую вероятность данного типа боли указывают симптомы «опасности» («красные флажки»): повышение температуры, травма в анамнезе, изменение веса тела за последний год, утренняя скованность, интенсивная ночная локальная боль, тазовые нарушения. При наличии одного из этих симптомов рекомендуется проводить неврологический и общесоматический осмотр, при необходимости – дополнительные лабораторные и диагностические обследования с привлечением узких специалистов.
После исключения специфической боли рекомендуется проводить дифференциальную диагностику неспецифической и корешковой боли в спине.
Неспецифическая скелетно-мышечная боль обусловлена механическим воздействием на связки, мышцы, сухожилия и фасции (мышечно-тонический или миофасциальный синдром), межпозвонковые диски, фасеточные суставы позвоночника (фасеточный синдром). Корешковая боль развивается в результате компрессии спинномозгового корешка или спинномозговых нервов [1–3]. Для проведения дифференциальной диагностики рекомендуется придерживаться следующего алгоритма обследования.
1. Оценить положение больного, осанку, позу, походку, объем движения.
При болевом синдроме возможно формирование анталгической позы, которая уменьшает интенсивность боли, разгружает компримированный корешок. Анталгические позы бывают самыми разными вследствие уплощения лордоза, увеличения кифоза или формирования сколиотической установки. Анталгическая поза меняет походку – больной может сгибать ногу в суставах, прихрамывать и т. п. Для определения объема движений мы рекомендуем использовать функциональные тесты Минора, Петелина, Попелянского, Отта, Шобера.
2. Определить интенсивность, локализацию и характер боли.
Наиболее чувствительным методом для количественной оценки боли является визуальная аналоговая шкала (ВАШ). Дополнительно используют вербальную шкалу (ВШ). Боль может быть локальной или диффузной с иррадиацией. Мышечно-тонический синдром при неспецифической боли – локальный. При миофасциальном синдроме боль может быть локальной или иррадиировать, но не по корешковому типу. Корешковая боль иррадиирует по ходу нерва. По классификации, предложенной Международной ассоциацией по изучению боли (IAPS, 1994), острая боль продолжается до 12 нед., хроническая – свыше 12 нед. Некоторые авторы выделяют период подострой боли – от 6 до 12 нед. [1–3].
3. Оценить мышечную силу и мышечный тонус.
Мышечная сила оценивается по 5-балльной шкале. Мышечный тонус определяется при пальпации, выделяют 3 степени напряжения мышц. Для мышечно-тонического синдрома характерны боль и повышение мышечного тонуса, который ограничивает объем движения в соответствующем двигательном сегменте. Мышечный тонус может быть локализован во всей мышце, отдельном ее участке или в нескольких мышцах. Боль уменьшается в покое и усиливается при движении. Для миофасциального синдрома характерны боль и наличие в одной или нескольких мышцах триггерных точек, которые представляют собой гипервозбудимую область, болезненную при пальпации. При корешковой боли возможны снижение мышечной силы и повышение мышечного тонуса. Мышечный спазм уменьшает подвижность нервных корешков, снижает их способность к растяжению. Проверяются следующие симптомы натяжения: Ласега, посадки, Бонне, Вассермана – Мацкевича, Нери, Дежерина.
4. Выявить сопутствующие симптомы.
Могут наблюдаться нарушения чувствительности: гиперестезия – повышение чувствительности; гиперпатия – извращенная чувствительность, отсутствует чувство локализации и отмечается неприятный оттенок ощущений; дизестезия – извращение чувствительности, при котором одно раздражение воспринимается как другое; парестезии – неприятные ощущения, возникающие без нанесения раздражений; анестезия – полная утрата того или иного вида чувствительности; сенестопатии (жжение, неприятные ощущения с психоэмоциональными наслоениями). При корешковой боли (при поражении заднего корешка) возможно нарушение всех видов чувствительности в соответствующем дерматоме. При неспецифической боли также могут быть нарушения чувствительности и сенестопатии.
5. Проверить сухожильные и периостальные рефлексы.
Исследование сухожильных и периостальных рефлексов важно для установления уровня поражения корешка или спинного мозга. Чаще отмечают понижение или выпадение рефлексов, но может быть гиперрефлексия, что указывает на симптомы раздражения определенных образований. При корешковом синдроме отмечается комплекс симптомов: боль, расстройство чувствительности, нарушение движения с развитием мышечной слабости вплоть до плегии, изменение тонуса и трофики мышц, снижение или полное отсутствие сухожильных рефлексов [1–3].
Далее для уточнения состояния позвоночника рекомендуется функциональная рентгенография с целью определения расположения позвонков, наличия аномалий и выраженности дегенеративно-дистрофического процесса. Необходимо учитывать, что нет четкой корреляции между выявленными изменениями и клинической картиной. При корешковом синдроме информативно нейровизуализационное исследование – магнитно-резонансная томография позвоночника (МРТ). МРТ отличается безвредностью и возможностью получить изображения с большой точностью, увидеть срезы позвоночного столба и спинного мозга, размеры и расположение грыжи. Алгоритм диагностики представлен на рисунке 1.
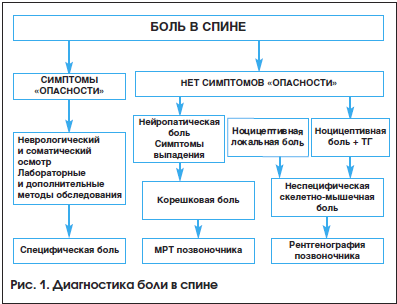
Лечение
В остром периоде важной задачей является купирование боли. Для этого назначаются нестероидные противовоспалительные препараты (НПВП). Они ингибируют циклооксигеназу (ЦОГ) – основной фермент метаболизма арахидоновой кислоты, оказывают противовоспалительное и обезболивающее действие. ЦОГ присутствует в организме в двух изоформах: ЦОГ-1 и -2. ЦОГ-1 находится во всех тканях и регулирует ряд физиологических функций. ЦОГ-2 синтезируется на фоне воспаления. По отношению к ЦОГ все НПВП разделяют на неселективные, или традиционные, селективные и высокоселективные. Неселективные НПВП ингибируют ЦОГ-1 и -2. Эта группа блокирует выработку простагландинов не только в очаге воспаления, но и в здоровых органах и клетках крови. В результате кроме положительного эффекта появляются побочные симптомы. Поскольку простагландины защищают слизистую желудка от агрессивного воздействия кислого желудочного сока, то при назначении традиционных НПВП высока вероятность развития гастропатий, повышен риск кровотечений. Возможны и другие побочные симптомы: снижение диуреза, тенденция к бронхоспазму, головокружение, повышение артериального давления.
Селективные НПВП ингибируют преимущественно ЦОГ-2, поэтому имеют улучшенный профиль безопасности. Производные оксикамов (мелоксикам) имеют ряд преимуществ по сравнению с другими селективными НПВП, не являются гепатотоксичными и не вызывают осложнений со стороны сердечно-сосудистой системы [4]. Мелоксикам имеет большой период полувыведения, максимальная концентрация (Cmax) в плазме после приема 15 мг препарата достигается через 7 ч, время полувыведения составляет 20–24 ч. Это позволяет назначать его 1 р./сут, что значительно повышает комплаентность пациентов. Мелоксикам обладает длительным обезболивающим эффектом. Он не оказывает ингибирующего действия на образование протеогликана и не увеличивает синтез интерлейкина-1, поэтому не влияет негативно на хрящ и считается хондронейтральным препаратом.
С целью оптимизации результатов лечения, усиления анальгезирующего действия рекомендуется в схему терапии включать витамины группы В. Они имеют сложный механизм действия. Витамин В1 (тиамин) улучшает проведение нервного импульса, обладает антиоксидантной активностью, играет роль коэнзима в цикле Кребса – основном цикле утилизации глюкозы с образованием энергии. Самостоятельно или в комбинации с витаминами В6 и В12 способен тормозить прохождение болевой импульсации на уровне задних рогов и таламуса, уменьшает интенсивность боли, парестезий, улучшает температурную и вибрационную чувствительность. Тиамин – это водорастворимая форма В1, она всасывается за счет активного транспорта, легко разрушается тиаминазой, поэтому не накапливается в организме. Жирорастворимая форма тиамина (бенфотиамин) эффективнее водорастворимой. Бенфотиамин всасывается за счет пассивной диффузии и обладает в 120 раз большей внутриклеточной биодоступностью, чем тиамин.
Витамин B6 (пиридоксин) является коферментом в метаболизме аминокислот, регулирует обмен нейромедиаторов норадреналина, дофамина и миелиновой ткани, участвует в синтезе транспортных белков и гамма-аминомасляной кислоты, которая является важнейшим тормозным нейромедиатором ЦНС человека. Витамин B6 оказывает влияние на трофические процессы в нервной ткани, создает условия для более успешной регенерации нервных волокон. Снижает болевые ощущения, связанные с поражением периферической нервной системы.
Витамин В12 (цианокобаламин) в организме метаболизируется в метилкобаламин, который образуется в результате распада гомоцистеина. После активизации реакции трансметилирования из метионина синтезируется промежуточный продукт – S-аденозил-метионин, затем из него – фосфатидилхолин. Фосфатидилхолин – одна из самых распространенных молекул, входящих в состав клеточных мембран. Таким образом, витамин В12 является необходимым веществом, стимулирующим процессы регенерации. Витамин В12 участвует в синтезе ДНК всех делящихся клеток, необходим для синтеза миелина, который входит в состав миелиновой оболочки аксонов ряда нейронов. Миелиновая оболочка выполняет не только защитные функции, но и ускоряет передачу нервных импульсов. Витамин В12 оказывает обезболивающее действие. Доказано, что терапия витаминами В1, В6 и В12 более эффективна, чем монотерапия одним из этих витаминов.
В комплексную терапию боли в спине при мышечном напряжении включают миорелаксанты. При боли на фоне дегенеративно-дистрофического процесса назначаются с первого дня обострения структурно-модифицирующие медленнодействующие препараты. При корешковой невропатический боли рекомендуются антиконвульсанты, среди которых хорошо себя зарекомендовал габапентин. Препарат имеет сложный механизм действия. Он оказывает модулирующее влияние на NMDA-рецепторы, блокирует α2δ-субъединицу кальциевых каналов, снижает высвобождение моноаминов, уменьшает синтез и транспорт глутамата, блокирует потенциалзависимые N-кальциевые каналы, что приводит к снижению боли, аллодинии и механической гиперсенситивности. Габапентин обладает высокой терапевтической эффективностью. При постепенном подборе оптимальной дозы методом титрации хорошо переносится, побочные явления не выражены [5].
При остром болевом синдроме развитие воспалительной реакции приводит к высвобождению провоспалительных цитокинов, местным расстройствам гемодинамики и лимфодинамики, повышению сосудистой проницаемости и, как следствие, – накоплению жидкости в межклеточном пространстве. Отек может вызвать метаболические нарушения, вторичное расстройство кровообращения, местную гипоксию тканей вплоть до некроза [6, 7]. Выраженным и быстрым противоотечным действием обладает препарат L-лизина эсцинат. Он состоит из аминокислоты L–лизина и тритерпеновых сапонинов конского каштана. L–лизина эсцинат оказывает анальгетическое и антиэкссудативное действие посредством нормализации повышенной сосудистой проницаемости. Ингибирование активности аутолитических ферментов предупреждает расщепление мукополисахаридов в стенках капилляров и в соединительной ткани, которая их окружает. Проявляя антагонизм в отношении брадикинина и серотонина, препарат нормализует капиллярную проницаемость, улучшает микроциркуляцию и лимфоотток, уменьшает выраженность экссудативного и воспалительного процесса [8, 9]. L-лизина эсцинат вводят строго в/в медленно капельно в суточной дозе 5 мл, предварительно разведя в 50–100 мл 0,9% раствора натрия хлорида. Длительность лечения – 5–10 дней в зависимости от динамики терапевтического эффекта.
L-лизина эсцинат также показал свою эффективность в лечении хронического болевого синдрома у пациентов с грыжами одного или нескольких поясничных межпозвонковых дисков (сопровождающихся расширением корешковых вен конского хвоста, эпидуральных вен, центральных вен тела позвонка). Применение препарата способствовало регрессу отека корешков и спинного мозга и связанных с венозным застоем неврологических проявлений [10].
Алгоритм медикаментозного лечения пациентов с болью в спине представлен на рисунке 2.
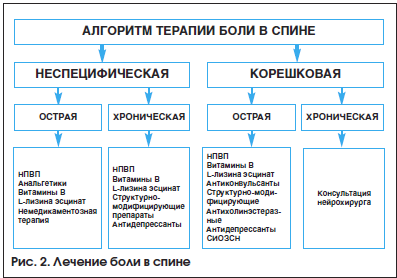
Из немедикаментозной терапии при боли в спине показаны физиотерапия, иглорефлексотерапия, мануальная терапия, массаж и лечебная гимнастика.
Таким образом, боль в спине различна по этиологии. Алгоритм диагностики включает комплексное обследование. Терапия боли в спине должна проводиться с учетом этиологии, патогенеза, стадии заболевания, клинического течения.
Источник
Дано определение боли в нижней части спины. Рассмотрены вопросы эпидемиологии, патогенеза, дифференциальной диагностики и лечения этого состояния. Подчеркивается, что комплексный подход, включающий как медикаментозные, так и немедикаментозные методы, в наибольшей степени позволяет управлять болью в нижней части спины. При этом медикаментозная терапия должна включать не только нестероидные противовоспалительные препараты, но и нейропротекторы, антидепрессанты, полинуклеотидные комплексы и препараты, обладающие метаболическими свойствами.
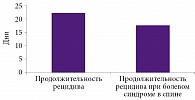
Рис. 1. Продолжительность рецидивов хронической боли в среднем и при болевом синдроме в спине в Российской Федерации
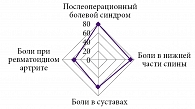
Рис. 2. Интенсивность болевого синдрома в зависимости от причин боли по визуальной аналоговой шкале, мм

Рис. 3. Болевой анамнез
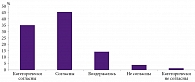
Рис. 4. Мнение международных экспертов по поводу назначения НПВП для купирования боли в спине
![Таблица. Степень доказательности врачебных интервенций при БНС [1]](https://umedp.ru/upload/resize_cache/iblock/5c8/195_350_1/bolvspine_tab.jpg)
Таблица. Степень доказательности врачебных интервенций при БНС [1]
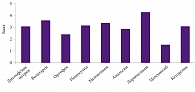
Рис. 5. Степень доверия врачей различным НПВП
Определение
Боль в нижней части спины (БНС) – это боль, мышечное напряжение и/или скованность, локализованные в области спины между XII парой ребер и нижними ягодичными складками с иррадиацией или без иррадиации в нижние конечности. Синдром БНС (доброкачественная скелетно-мышечная боль в спине) не считается нозологической единицей. Ввиду высокой распространенности и невозможности установить конкретную анатомическую причину боли у большей части пациентов в Международной классификации болезней 10-го пересмотра синдрому БНС присвоен статус регистрационной категории М54.5.
По данным большинства зарубежных рекомендаций, нет четкой связи между выраженностью морфологических изменений позвоночника и наличием/выраженностью боли в спине, что особенно актуально именно для неспецифической БНС (М54.5). В частности, при проведении магнитно-резонансной томографии патология межпозвонковых дисков нередко обнаруживается у практически здоровых людей, а клинические исследования неоднократно демонстрировали, что выявление патологических изменений в межпозвонковом диске не предрасполагает к развитию боли в спине при дальнейшем наблюдении обследуемых [1].
Эпидемиология
Боль в области спины широко распространена в популяции, ее испытывают преимущественно люди трудоспособного возраста. В течение жизни боль в спине возникает у 70–90% населения, а у 20–25% регистрируется ежегодно [2].
По результатам большого проекта по изучению заболеваемости населения на глобальном уровне (Global Burden of Disease Study), именно боль в спине является главной причиной нетрудоспособности в мире [3]. Боль в нижней части спины остается одной из самых частых причин обращения за медицинской помощью, причем сегодня пациенты приходят за облегчением боли к врачам разных специальностей.
Проблема боли в спине актуальна в первую очередь в связи c недостаточной эффективностью лечения. Важность и сложность адекватного обезболивания в реальной клинической практике определяются коморбидностью, полипрагмазией и необходимостью планирования долгосрочной терапии болевого синдрома [4].
Ряд эпидемиологических исследований подтверждает эффективное обезболивание лишь у пятой части пациентов. Это обусловлено использованием малоэффективных лекарственных средств, стандартных либо устаревших схем их применения, рефрактерностью у пациентов, часто использующих анальгетики, нежелательными побочными реакциями и др. [5].
У подавляющего большинства пациентов в результате проводимой терапии боли купируются в течение четырех недель. Вместе с тем у 73% больных в течение первого года развивается как минимум одно обострение [2]. В 20–25% случаев боль в спине переходит в хроническую стадию, причем на эту категорию больных приходится до 80% экономических затрат [6]. В одном из европейских многоцентровых исследований показано, что хронической болью страдает каждый пятый житель Европы, большинство пациентов испытывало боль именно в нижней части спины [7].
Патогенез
К основным вертеброгенным причинам болевого синдрома относятся дегенеративно-дистрофические заболевания в межпозвонковых дисках и мышечно-связочном аппарате позвоночника, которые проявляются снижением гидрофильности и деструкцией ткани межпозвонковых дисков, их грыжевидным выпячиванием в сторону позвоночного канала, реактивными изменениями в прилежащей костной ткани позвонков и сопровождаются артрозом дугоотростчатых суставов.
Вертеброгенные болевые синдромы (дорсалгии) возникают в результате негативного взаимодействия измененных дистрофическим процессом тканей опорно-двигательного аппарата и провоцирующих факторов. К последним относятся мышечное перенапряжение, подъем или перенос тяжести, длительное пребывание в неудобной позе, переохлаждение, эмоциональный стресс и пр.
Следует отметить весомую роль психогенных факторов в развитии боли. Так, наличие боли приводит к развитию депрессивных состояний, которые в свою очередь способствуют поддержанию и усилению болевого феномена. Этот замкнутый круг нередко лежит в основе хронизации болевых синдромов [8].
Боль в нижней части спины: изучение российской клинической практики
Нами было проведено многоцентровое исследование [9], посвященное оценке ведения пациентов с болевым синдромом в практике врачей терапевтических специальностей, неврологов и хирургов. Предметом интереса исследования явились эпидемиологические сведения о хронической боли в РФ.
В исследование были включены 950 пациентов (33,2% мужчин и 66,8% женщин) из Москвы, Московской области, Воронежа, Астрахани, Липецка, Санкт-Петербурга, Сочи, Кирова, Кировской области. Пациенты наблюдались у 275 врачей различных специальностей. Средний возраст пациентов составил 52,6 года. Статистически достоверной разницы между возрастом мужчин и женщин не было. 21,2% пациентов имели инвалидность, преимущественно ΙΙ группы.
Следует подчеркнуть, что чаще всего боль локализовалась в спине (57,6–60,6%). Согласно результатам анализа медицинской документации, боль в спине объяснялась дорсопатией (n = 417, 72,4%) и грыжей межпозвоночного диска (n = 104, 18,1%). Описанные выше причины боли в спине практически не указывались. Только в 34 (5,9%) случаях были зафиксированы остеопоротические переломы тел позвонков, а в 21 (3,6%) – другие причины. При этом в историях болезни и амбулаторных картах мы не нашли исследований, необходимых для дифференциальной диагностики боли в спине. Следовательно, в Российской Федерации уточнение генеза боли в спине практически не проводится, хотя это и не требует значимых экономических затрат.
У пациентов с болью в спине продолжительность последнего рецидива боли составила 17,6 ± 14,7 дня (рис. 1). В среднем первый болевой опыт отмечен больными в 35,2 года (минимальный показатель – 23, максимальный – 54 года). Средняя продолжительность хронической боли составила 9,4 ± 5,7 года.
Следует обратить внимание практикующих врачей на тот факт, что интенсивность боли в спине достоверно не отличается от таковой при послеоперационном болевом синдроме, который традиционно используется как модель интенсивной боли (рис. 2).
Дифференциальная диагностика
Следует остановиться на значимости боли в спине прежде всего c клинической точки зрения. Традиционно в отечественной клинической практике боль в спине ассоциируется только c дегенеративно-дистрофическими заболеваниями позвоночника. Это изначально сокращает объем дифференциальной диагностики данного симптома. Современное представление о боли в спине следует преломить в сферу более актуальных медико-социальных проблем.
Аневризма брюшного отдела аорты
Наиболее распространенной патологией в современной популяции являются сердечно-сосудистые болезни, которые обусловливают более 55% смертельных исходов. Этот факт имеет особое значение и для клинической оценки больных c болью в спине.
Аневризма аорты встречается примерно у одного из 20 человек старше 65 лет. Боль в спине может вызвать эрозия позвонков, обусловленная большой аневризмой брюшной аорты. Речь идет именно об аневризмах значительного размера. Основной вклад, несмотря на многофакторность патологии, в увеличение размеров аневризмы вносит атеросклероз, на счет которого можно отнести около 90% всех случаев аневризмы брюшной аорты. Начало заболевания, как правило, бессимптомное. Первые проявления отмечаются, когда увеличивающаяся аневризма начинает давить на прилегающие органы, в том числе позвонки. Соответственно боль в спине может стать дебютным симптомом. В этой связи при наличии боли в спине, клинических признаков атеросклероза необходимо исключить аневризму брюшного отдела аорты.
Метастатическое поражение позвонков
Еще одной достаточно частой причиной болевого синдрома в спине являются метастазы в тела позвонков.
Под нашим наблюдением был мужчина 65 лет, поступивший в стационар скорой помощи по поводу боли в спине. Это было первое обращение пациента за медицинской помощью за последние 15 лет. В неврологическом отделении у больного была диагностирована дорсопатия, по поводу которой назначены нестероидные противовоспалительные препараты (НПВП). На третьи сутки пребывания в стационаре пациент погиб от массивного желудочно-кишечного кровотечения. У пациента был обнаружен центральный рак правого легкого c метастазами в тела поясничных позвонков L1–L3, язва крупных размеров в слизистой оболочке желудка.
Онкологические заболевания занимают второе место в структуре смертности в популяции. Анализ литературы свидетельствует о том, что у 5–10% всех онкологических больных имеет место метастатическое поражение позвоночника. Причем у 8–47% пациентов боль при метастатическом поражении позвонков является первым симптомом онкологического заболевания, поэтому при проведении дифференциального диагноза боли в спине врачу необходимо задуматься о возможной онкологической патологии [10]. Следует обращать внимание на такие знаки-угрозы, как снижение массы тела, неэффективность терапии, пожилой возраст, анемия и т.п.
Туберкулез позвоночника
Причиной боли в спине могут быть инфекционные процессы, среди которых лидирует туберкулез позвоночника. Подозревать инфекционный процесс можно при наличии лихорадки, внутривенном введении лекарств (в том числе наркотиков) в анамнезе, имеющемся инфекционном процессе мочевыводящих, дыхательных путей, кожи, а также иммунодефицитных состояниях и боли в покое.
Компрессионный перелом тел позвонков при остеопорозе
Наиболее частой причиной боли в спине в современной популяции являются остеопоротические осложнения – переломы тел позвонков.
По самым скромным подсчетам, в Российской Федерации около 15 млн человек страдает остеопорозом. Как показали наши исследования распространенности остеопороза (n = 8600), у более 72% соматических больных определяется низкая минеральная плотность костной ткани. Следует подчеркнуть, что наличие компрессионных переломов слабо коррелирует c Т-критерием, полученным при денситометрии. Другими словами, даже при незначительных потерях минеральной плотности костной ткани может констатироваться перелом позвонков. Одним из быстрых и удобных маркеров остеопоротического перелома является снижение роста более чем на 3 см.
Предполагать наличие остеопороза следует практически в каждом случае болевого синдрома в спине. При наличии факторов риска остеопороза необходимо провести рентгенологическое исследование позвоночника c прицельным изучением компрессии тел позвонков.
К другим более редким причинам боли в спине, однако имеющим особое значение в сравнении c первичными причинами (дегенеративные изменения межпозвоночного хряща и спондилоартроз), следует отнести синдром Рейтера, ревматоидный артрит, острые нарушения спинального кровообращения, отраженные боли при заболеваниях органов малого таза (в том числе почечная колика, гинекологические заболевания).
Лечение
Принципиально важно при ведении пациентов с болью в спине тщательно собрать болевой анамнез (рис. 3). Тактика лечения пациента с хронической БНС (основанная на принципах доказательной медицины) включает:
1) информирование пациента о причинах боли в спине и, как правило, ее доброкачественной природе;
2) исключение постельного режима с обеспечением достаточного уровня повседневной активности;
3) назначение доказанного эффективного лечения (в первую очередь для устранения боли);
4) коррекцию тактики ведения при ее неэффективности в период 4–12 недель.
Согласно международным рекомендациям, в лечении хронической БНС наиболее эффективны НПВП, трициклические антидепрессанты, психотерапия, лечебная физкультура, мануальная терапия [1].
Исходя из практических рекомендаций по ведению хронической боли большинство международных экспертов считают обязательным применение НПВП для купирования боли в спине (рис. 4, таблица) [11]. Был проведен опрос врачей о назначении различных НПВП, при этом обрабатывались только те ответы, в которых указывались как минимум три препарата. В результате был составлен список наиболее часто упоминаемых лекарственных средств: лорноксикам, кеторолак, анальгин, нимесулид, мелоксикам, диклофенак натрия, целекоксиб (рис. 5).Торговые наименования диклофенака натрия были выделены отдельно, поскольку доверие врачей к оригинальному препарату было достоверно выше по сравнению с дженериками. Наибольшую степень доверия мы констатировали у препарата лорноксикам – 4,3 ± 0,5 балла, наименьшую – у целекоксиба – 1,6 ± 0,3 балла (р
При длительном персистирующем течении вертеброгенные болевые синдромы могут приобретать черты нейропатического болевого синдрома, что предполагает применение помимо противоболевой терапии антидепрессантов и антиконвульсантов.
Известно, что развитие нейропатического компонента болевого синдрома связано с сегментарной демиелинизацией корешкового аппарата, которая приводит к дисбалансу в процессе прохождения потоков импульсов по быстро- и медленнопроводящим чувствительным волокнам, нарушая систему контроля «ворот» боли. Данное положение обусловливает необходимость включения в схемы лечения вертеброгенной боли нейропротекторной терапии для защиты поврежденных нейронов, основу которой составляют препараты с метаболическим, нейротрофическим и восстановительным свойством. Одним из высокоэффективных метаболических препаратов является Актовегин. Основное действие Актовегина заключается в повышении внутриклеточного транспорта и утилизации глюкозы и кислорода, активации процессов аэробного окисления, стабилизации энергетического потенциала клеток [12].
Активная фракция препарата характеризуется инсулиноподобным эффектом. Следует подчеркнуть, что антитела к инсулину не блокируют этот эффект и не нарушают транспорт глюкозы, который под влиянием Актовегина усиливается в пять, а не в десять раз, как под воздействием инсулина. Показано, что инсулиноподобное действие оказывают выделенные из Актовегина инозитолфосфат-олигосахариды, активирующие переносчики глюкозы в плазматической мембране.
Актовегин обладает антигипоксантным эффектом за счет активации ряда ферментов окислительного фосфорилирования и является мощным непрямым антиоксидантом, увеличивая активность ключевого фермента антиоксидантной системы – супероксиддисмутазы [12]. Нормализация эндотелиальной функции на фоне приема Актовегина способствует улучшению перфузии органов и тканей за счет нормализации периферического сосудистого сопротивления.
Под влиянием препарата значительно улучшается диффузия кислорода в нейрональных структурах, что позволяет уменьшить выраженность трофических расстройств [13]. Отмечаются также значительное улучшение периферической микроциркуляции, вазодилатация на фоне улучшения аэробного энергообмена сосудистых стенок и высвобождения простациклина и оксида азота (вторичный эффект).
В ряде исследований было показано, что использование Актовегина при болях в спине способствует нормализации метаболических и обменных процессов в структурах позвоночно-двигательного сегмента и корешковом аппарате, устранению триггерных зон и предотвращению развития приступа боли [14].
В исследовании Ю.В. Кислицына на фоне десятидневного введения Актовегина 400 мг внутривенно доля пациентов с интенсивной болью в спине сократилась на 36,6% [15].
Учитывая, что для восстановления миелиновой оболочки корешков и нервов требуется повышенное снабжение организма нуклеотидами, в схемы восстановительной терапии при вертеброгенной боли целесообразно включать современный полинуклеотидный комплекс Келтикан, содержащий цитидин-5-монофосфат и уридин5-трифосфат. Метаанализ рандомизированных плацебоконтролируемых исследований показал, что использование полинуклеотидных комплексов увеличивает площадь поверхности миелина и толщину аксона, стойко улучшает скорость проведения импульса по нервному волокну, а также способствует сокращению выраженности болевого синдрома у больных с цервикалгией, люмбалгией, диабетической невропатией и невралгией [16–18]. Использование комплекса нуклеотидов (Келтикан) позволяет восстановить структуру спинальных корешков, что приводит к сбалансированности прохождения по ним афферентных потоков импульсов разной модальности и способствует «закрытию ворот» для потока болевой импульсации [18].
Психические нарушения могут не только поддерживать хроническую боль и формировать связанную с ней инвалидизацию, но и повышать риск развития боли в спине. По мнению целого ряда авторов, психологические факторы вносят больший вклад в развитие инвалидизации, связанной с болью в спине, чем биомеханические нарушения позвоночника и суставов конечностей. Данные обстоятельства обусловливают необходимость включения антидепрессантов в комплексное лечение хронической боли в спине.
Таким образом, эффективное купирование хронической боли в спине возможно только при планировании длительной терапии, включающей как немедикаментозные, так и медикаментозные методы. При этом медикаментозное лечение должно включать не только НПВП, но и нейропротекторы, антидепрессанты, полинуклеотидные комплексы. Именно такая комбинированная терапия в наибольшей степени позволяет управлять болью.
Источник
